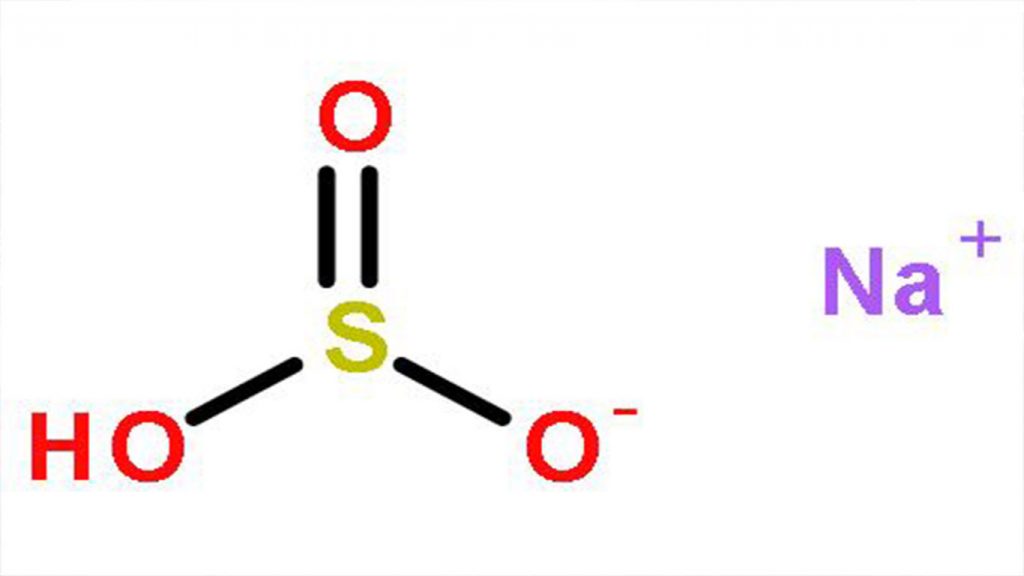
Natri bisunfit hay natri hiđrosulfit là một hợp chất vô cơ có công thức hóa học là NaHSO3, tồn tại dạng chất bột kết tinh màu trắng, có mùi khó chịu do lưu huỳnh đioxit.
Mục lục
Thông tin về sản phẩm Natri bisunfit NaHSO3
– Tên gọi: Natri bisulfit, bisulfit natri, natri hiđrosulfit; Sodium bisulfite
– Quy cách: 25kg/bao
– Xuất xứ: Trung Quốc
(Bao bì Natri bisulfit NaHSO3 xuất xứ Trung Quốc)
– Hàm lượng: 99%
Tính chất vật lý và hóa học của natri hiđrosulfit NaHSO3
Tính chất vật lý của NaHSO3
– Khối lượng mol là 104.061 g/mol
– Khối lượng riêng là 1.48 g/cm3
– Nhiệt độ nóng chảy là 150 °C (423 K; 302 °F)
(Ảnh minh họa hóa chất NaHSO3)
– Độ hòa tan trong nước là 42 g/100 mL
– Dễ tan trong nước nhưng khó tan trong rượu.
Tính chất hóa học của NaHSO3
– NaHSO3 là muối của axit và là chất điện li mạnh khi tan trong nước.
- NaHSO3 → Na+ + HSO3–
- HSO3– ⇌ H+ + SO32-
– Ở nhiệt độ phòng quá trình phân hủy NaHSO3 diễn ra chậm. Dưới xúc tác là độ ẩm phản ứng phân hủy sẽ diễn ra nhanh hơn.
- 2NaHSO3 → Na2SO3 + SO2 + H2O
(Cấu tạo phân tử Natri bisulfit – NaHSO3)
– Natri bisulfit tác dụng với kẽm tạo ra natri hiđrosunfit
- 4NaHSO3 (đậm đặc) + Zn → Na2S2O4 + Na2SO3 + ZnSO3 + 2H2O
- 2NaHSO3 + Zn + H2SO3 → Na2S2O4 + ZnSO3 + 2H2O
- 2NaHSO3 + Zn + SO2 → Na2S2O4 + ZnSO3 + H2O
– Dung dịch natri bisulfit tác dụng của axit tạo thành muối natri của axit tương ứng, đồng thời giải phóng khí lưu huỳnh đioxit.
- NaHSO3 + H2SO4 →Na2SO4 + 2SO2 + 2H2O
- NaHSO3 + HCl → NaCl + SO2 + 2H2O
– Bisulfit natri phản ứng với clo hoặc iốt để tạo ra natri sunfat và axit hydrohalic hoặc halogenua.
- NaHSO3 + Cl2 + H2O → NaHSO4 + 2HCl
- NaHSO3 + I2 + H2O → NaHSO4 + 2HI
– Sodium bisulfite phản ứng với kiềm, muối hoặc hợp chất hữu cơ để tạo ra các sản phẩm khác nhau.
- NaHSO3 + NaOH → Na2SO3 + H2O
- 2NaHSO3 + NaNO2 → Na2HNS2O7 + NaOH
- 5NaHSO3 + 2KIO3 + 2H2SO4 → 5NaHSO4 + 2KHSO4 + I2 + H2O
Phương thức sản xuất natri hiđrosulfit NaHSO3
– Dẫn khí lưu huỳnh đioxit (SO2) qua dung dịch soda (Na2CO3), phản ứng kết thúc đem dung dịch này ly tâm và làm khô trong không khí ở nhiệt độ 250-300 °C ta thu được thành phẩm là natri bisulfit 99%
- Na2CO3 + 2SO2 + H2O → 2NaHSO3 + CO2 ↑
(Nhà máy sản xuất NaHSO3 tại Trung Quốc)
– Na2CO3 dạng rắn được cho vào dung dịch NaHSO3 (nồng độ 40%, PH 3-4) tạo thành dung dịch Na2SO3 tiếp tục dẫn khí SO2 vào bằng cách đốt lưu huỳnh. Kết thúc phản ứng tạo kết tủa tiến hành ly tâm thu natri bisulfit ướt có độ ẩm 6-10% tiếp tục làm khô để tạo ra NaHSO3 khan.
- 2NaHSO3 + Na2CO3 → 2Na2SO3 + H2O + CO2 ↑
- Na2SO3 + H2O → 2NaHSO3
Ứng dụng của bisulfit natri NaHSO3
NaHSO3 – natri hiđrosulfit được ứng dụng trong ngành công nghiệp dệt nhuộm
– NaHSO3 được sử dụng là chất tẩy trắng vải bông (vải hữu cơ)
– Được sử dụng như một chất khử trong thuốc nhuộm, sản xuất giấy, thuộc da
Natri bisulfit được ứng dụng trong ngành công nghiệp thực phẩm
– NaHSO3 được dùng trong sản xuất rượu vang thương phẩm, giúp các chai rượu ngăn được sự hình thành giấm chua do vi khuẩn và là chất oxy hóa giúp giữ hương vị, mùi của rượu khỏi các biến đổi hoá học.
– Sodium bisulfite được ứng dụng giúp tẩy trắng thực phẩm do nó ức chế mạnh enzym oxidase trong thực phẩm là thực vật, tiêu diệt vi khuẩn giúp thực phẩm bảo quản lâu hơn.
– Sử dụng bisulfit natri cho sản xuất kẹo trái cây ,đường, đường phèn, caramel, glucose lỏng, trái cây sấy khô, rau khô, miến, măng, nấm và nấm đóng hộp với hàm lượng sử dụng tối đa là 0,45 g/kg.
– Natri bisulfi được sử dụng cho các sản phẩm thực phẩm thành phần chính là tinh bột khoai tây,với hàm lượng sử dụng tối đa 0,2g/kg.
Các ứng dụng khác của Natri bisulfit
– Trong ngành công nghiệp dược phẩm NaHSO3 được sử là chất trung gian dùng để sản xuất của Analgin và Aminopy.
– Natri hiđrosulfit được dùng là chất phụ gia mạ kim loại (Đồng, Niken, Kẽm, …)
– Natri bisulfit được sử dụng là chất chống ăn mòn oxi hóa trong các đường ống.
– Ngoài ra, Sodium bisulfite được sử dụng để xử lý nước thải có hàm lượng crom lớn và duy trì điều kiện thiếu không khí trong các lò phản ứng hóa sinh.
Những lưu ý khi sử dụng hóa chất NaHSO3
– Sử dụng Natri bisulfit trong thực phẩm cần tuân thủ hàm lượng hóa chất tối đa này cho phép, nếu sử dụng nhiều hơn có thể dẫn đến ngộ độc nguy hiểm.
– NaHSO3 không tự cháy tuy nhiên khi tiếp xúc với nguồn nhiệt sẽ diễn ra phản ứng cháy tạo ra khí SO2 độc hại.
– NaHSO3 là một hóa chất nguy hiểm, gây kích ứng cho da và mắt. Khi tiếp xúc với hóa chất cần trang bị đầy đủ đồ bảo hộ như: kính, mũ, khẩu trang lọc bụi, găng tay, ủng cao su,…
– NaHSO3 cần được bảo quản trong kho kho ráo, thoáng mát, thông gió. Tránh xa lửa, nguồn nhiệt và ánh nắng trực tiếp. Không bảo quản Sodium bisulfite chung với chất oxy hóa, axit và kiềm.
– Không nên bảo quản NaHSO3 trong thời gian dài để tránh bị biến chất làm ảnh hưởng đến chất lượng hóa chất khi sử dụng.
Natri Bisunfit
Thông tin liên hệ
🏢 Về Chúng Tôi – Công Ty Cổ Phần VCS Việt Nam
Công ty Cổ phần VCS Việt Nam là đơn vị uy tín hàng đầu trong lĩnh vực cung cấp hóa chất công nghiệp, thiết bị phòng thí nghiệm và giải pháp xử lý cáu cặn – ăn mòn hệ thống. Với hơn 10 năm kinh nghiệm, chúng tôi tự hào là đối tác tin cậy của hàng nghìn doanh nghiệp, nhà máy và cơ sở sản xuất trên toàn quốc. VCS cam kết mang đến những sản phẩm an toàn – hiệu quả – thân thiện môi trường, cùng dịch vụ tư vấn kỹ thuật chuyên sâu, đáp ứng mọi nhu cầu từ dân dụng đến công nghiệp.